Problema 5.1.4
Determinare l’equivalente in acqua di un calorimetro delle mescolanze, sapendo:
– la massa iniziale dell’acqua m1=150g;
– la temperatura iniziale del sistema acqua- calorimetro t1=32°C;
– la massa di acqua versata, a temperatura t2=45°C, nel calorimetro m2=100g;
– la temperatura di equilibrio te=37°C.
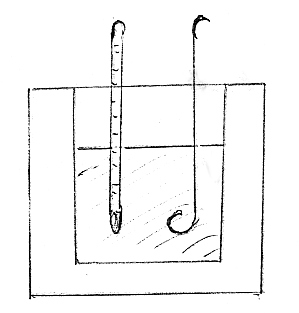
Il calorimetro delle mescolanze è costituito schematicamente da un recipiente con pareti isolate termicamente (per esempio un thermos) e con un coperchio che permette di utilizzare un termometro e un agitatore. Nel recipiente si trova una massa nota di acqua di cui si misura la temperatura di equilibrio iniziale. Nell’acqua si inserisce poi l’oggetto in esame e si aspetta fino a quando non si raggiunge la nuova temperatura di equilibrio.
Una volta nota la capacità termica del calorimetro, espressa in equivalente in acqua, è possibile calcolare in modo corretto il calore assorbito dal sistema calorimetro-acqua.
La quantità di calore ceduta dall’acqua versata nel calorimetro è Q=cm2(t2-te)
La quantità di calore assorbita dall’acqua contenuta nel calorimetro è Q1=cm1(te-t1)
La quantità di calore assorbita dal calorimetro è Q-Q1=K(te-t1) dove K è la capacità termica del calorimetro che equivale alla capacità termica di una massa di acqua equivalente me: cme=K.
Il sistema acqua-calorimetro ha quindi una capacità termica c(m1+me)
Otteniamo:
cm2(t2-te)=c(m1+me)(te-t1)
In questo modo possiamo ricavare l’equivalente in acqua del calorimetro me, che potrà essere utilizzato tutte le volte che usiamo questo calorimetro.
me=m2(t2-te)/(te-t1)-m1
Si ottiene per la massa equivalente del calorimetro me=10g.