Problema 12.5.9
Una massa m=16g di O2, inizialmente alla temperatura T1=600K e pressione p1=1,0 atm, compie il seguente ciclo reversibile:
1) trasformazione isobara fino a raggiungere la temperatura T2 = 2/3 T1;
2) compressione adiabatica durante la quale il volume si riduce alla metà (V3 = V2/2);
3) trasformazione isocora fino al punto 4;
4) trasformazione adiabatica che riconduce il gas alla condizione iniziale.
Calcolare:
a) Il rendimento del ciclo
b) La variazione di energia interna nelle singole trasformazioni
c) Il lavoro ottenuto dal ciclo (in joule)
d) La variazione di entropia nele singole trasformazioni.
|
Vedi soluzione del Problema 12.5.7. M=32 g/mole
1-2) isobara
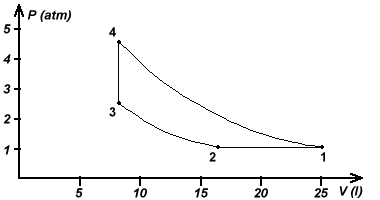 4-1) Adiabatica: p1V1γ = p4V4γ 3-4) isocora: T4=T3P4/P3
Calcolo del rendimento del ciclo: |