Supponiamo di far compiere reversibilmente a n=0,1moli di un gas perfetto biatomico il ciclo composto dalle seguenti trasformazioni, partendo dallo stato A (pA=500tor, VA=2,0dm3):
1) trasformazione isocora AB, in cui il rapporto di compressione è pB/pA=2;
2) trasformazione BC in cui la pressione è una funzione lineare del volume (vedi fig.12.13);
3) trasformazione isobara CA in cui il rapporto di espansione è VC/VA=1,5.
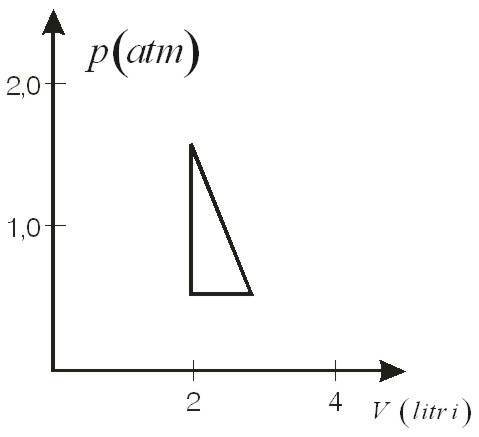 fig.12.13
fig.12.13Calcolare:
a) il rendimento del ciclo;
b) il calore ceduto dal gas durante la trasformazione BC (espresso il calorie).
|
Guarda la soluzione
|
a) Calcoliamo le coordinate termodinamiche degli stati A, B, C.
|
|
p (atm) |
V (l) |
T (K) |
Stato A |
Applichiamo l’eq.caratteristica dei gas perfetti pV=nRT:
T1=pAVA/nR
pA=500tor=500/760=0,66atm
TA=0,66.2/(0,082.0,1)=161K |
0,66 |
2,0 |
161 |
Stato B |
Trasf. Isocora:
pB=2pA=1,32 atm
TB/TA=pB/pA
TB= 322K |
1,32 |
2,0 |
322 |
Stato C |
VC/VA=1,5
VC=3l
TC/TA=VC/VA
TC= 242K |
0,66 |
3,0 |
242 |
Il rendimento è η=L/Q (Cap.12.5 b)) dove L è il lavoro fatto dal ciclo e Q il calore fornito dall’ambiente. In questo caso L si ottiene calcolando l’area racchiusa dal ciclo in fig.12.13:
L=(VC-VA).(pB-pA)/2
Q=QA.B=nCv(TB-TA) (isocora)
Cv=5R/2 (gas biatomico)
R=1,98cal/moleK
η=[(VC-VA).(pB-pA)/2]/nCV(TB-TA)
η=(1.0,66/2)/(0,1.2,5.1,98.161)=10%
b) Qc=Qf -Qas
Qf =QA,B=80cal è il calore fornito, Qas è il calore assorbito e Qc il calore ceduto.
Qas=L=10%Qf
Qas=8cal
Qc=80-8=72cal
QBC=Qc-QCA
QCA=nCp(TA-TC) (isobara)
Cp=7R/2
QCA=-56cal
QBC=72-56=16cal
Il gas cede calore sia nella trasformazione BC (-16cal) che nella CA (-56cal).
|
|
