Calcolare le coordinate termodinamiche nei punti 1,2,3 e le variazioni di energia interna, nel seguente ciclo reversibile condotto con un gas perfetto monoatomico.
1 à 2 isobara p1=1,0 atm ; V1=4,0 litri ; T1=300K
2 à 3 isocora V2=2,0V1 ; p3=1/2p2
3 à 1 isoterma
|
Guarda la soluzione
|
Applico l’equazione di stato dei gas perfetti (Cap.12.1) per calcolare il numero delle moli:
n=pV/RT
n=1,0.4,0/0,082.300=0,16 moli
a) Calcolo le coordinate termodinamiche.
|
p (atm) |
V (l) |
T (K) |
|
Stato 1 |
1,0 |
4,0 |
300 |
|
Stato 2 |
1,0 |
8,0 |
600 |
(isobara , se V raddoppia, raddoppia anche T) |
Stato 3 |
0,5 |
8,0 |
300 |
(isocora, se p dimezza, dimezza ancheT) |
Poi ritorna nelle condizioni iniziali con una trasformazione isoterma (figura).
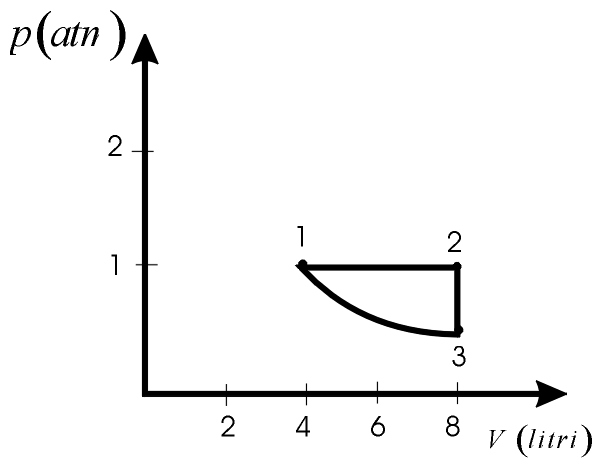
b) Vedi Problema 12.4.1.
ΔU=nCVΔT
nCV=0,16.3/2.8,31=2,0J/K (gas monoatomico)
ΔU1,2=2,0.300=600J
ΔU3,1=0 (trasformazione isoterma)
ΔU2,3=-ΔU1,2=-600J
Non importa fare il calcolo, sappiamo che la variazione di energia interna in un ciclo è zero (U è una funzione di stato).
|
|
