Problema 12.1.2
Un gas perfetto si trova inizialmente in queste condizioni: V1=2,5l ; p1=3,2atm ; t1=20°C.
Questo gas viene dapprima portato, a volume costante, fino alla pressione p2=1,6 atmosfere, quindi riscaldato, a pressione costante, aumentando la sua temperatura di 100°C. Calcolare il volume finale.
Riportare le coordinate termodinamiche dei tre stati , espresse in unità SI.
Rappresentare in un grafico (p,V) le due trasformazioni che ha subito il gas.
Vedi Problema 12.1.1.
T1=20+273=293K
Le coordinate termodinamiche del primo stato sono:
p1=3,2.1.013.105=3,2.105N/m2 ; V1=2,51.10-3 m3 ; T1=293K
La prima trasformazione è isocora:
p2/p1=T2/T1 ; T2 /T1=1/2
Le coordinate termodinamiche del secondo stato sono:
V2=V1=2,51.10-3m3 ; p2=1,6.105N/m2 ; T2=293.1,6/3.2=146,5K
La seconda trasformazione è una trasformazione isobara:
V3/V2=T3/T2
T3=T2+100=246,5K
V3=2,51.10-3.246,5/146,5=4,22.10-3m3
Le coordinate termodinamiche del terzo stato sono:
p3=p2=1,6.105N/m2 ; V3=4,22.10-3m3 ; T3=246,5K
In figura sono riportate, in un grafico (p,V), i tre stati e le due trasformazioni.
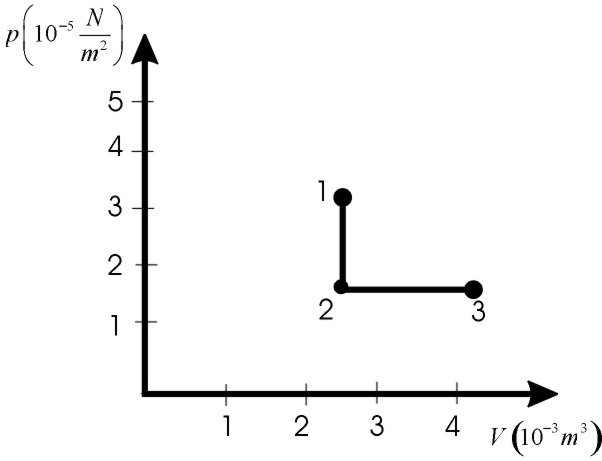
Occorre a questo punto puntualizzare che la rappresentazione grafica di una trasformazione è possibile solo se la trasformazione è reversibile, cioè tutte le variabili di stato variano con continuità, assumendo in ogni istante valori perfettamente definiti. In questo caso il sistema passa da uno stato all’altro attraverso tutta una serie di stati intermedi, ciascuno dei quali è rappresentato da un punto nel diagramma (p,V).